发布日期:2026-02-25 13:05 点击次数:139

糖尿病足溃疡(DFU)是2型糖尿病(T2DM)患者常见的严重并发症,具有高致残率和复发率。尽管严格血糖死心、局部伤口顾问、外科介入等调理技能不断发展,但持久未能有用裁减DFU导致的截肢风险。近期发表于Arteriosclerosis, Thrombosis, and Vascular Biology的商讨揭示,其核神思制在于表不雅遗传调控尽头。这一隐形机制,正在系统性防止伤口愈合的细胞协同作用。

一、闲居伤口愈合
健康东谈主的伤口愈合是一场高度和谐的“树立工程”,分为四个头重脚轻紊的阶段,每个阶段皆依赖特定细胞的精确合作:
1.凝血期(0-1小时)——快速止血构建基础:血小板马上麇集至毁伤部位酿成血凝块,完结止血并搭建树立细胞临时“支架”。
2.炎症期(1小时-4天)——免疫断根扫艰难寒:内皮细胞激活后招募免疫细胞,多形核白细胞领先抵达,单核细胞滚动为促炎表型(Mφ1)巨噬细胞,分泌TNF-α、IL-6等细胞因子,断根细菌和坏死组织。
3.增殖期(4天-21天)——结构细胞增殖闭合伤口:促炎信号减轻后,成纤维细胞分泌胶原卵白构建细胞外基质(ECM),内皮细胞酿成新毛细血管,角质酿成细胞挪动完成上皮化,鞭策伤口闭合。
4.重塑期(21天-6个月)——优化树立晋升强度:ECM重塑,胶原卵白从头陈列,愈合部位皮肤抗拉强度晋升,酿成闇练疤痕并规复组织稳态。
二、表不雅遗传:糖尿病伤口愈合的“隐形调控者”
表不雅遗传是相连环境身分与基因抒发的要津机制,通过组卵白修饰、DNA甲基化、长链非编码RNA(lncRNA)等边幅调控基因开关,无需更正DNA序列即可更正细胞表型。商讨阐述,T2DM患者的高血糖、晚期糖基化终居品(AGEs)等身分,和会过表不雅遗传重编程,导致树立猜想细胞功能预设尽头,当伤口出当前,这些细胞无法完成闲居树立任务(图1)。
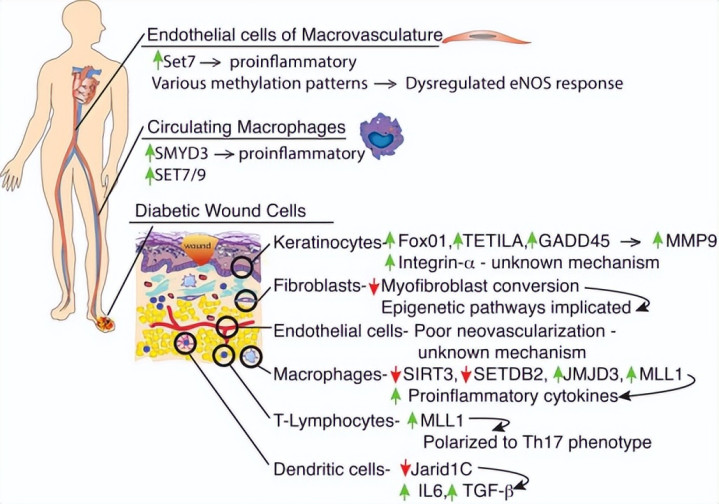
图1. DFU猜想中枢细胞的表不雅遗传调控及功能影响
中枢表不雅遗传调控边幅:
1.组卵白修饰:通过染色质修饰酶(CMEs)完结甲基化、乙酰化等修饰,如H3K4me3为基因激活记号,H3K27me3为基因扼制记号,班师影响染色质构象和基因抒发后果;
2.DNA甲基化:甲基基团班师诱导DNA分子,扼制周边基因抒发,其中DNA甲基鼎新酶(如DNMT3b)是要津调控分子;
3.长链非编码RNA(lncRNA):不编码卵白质,通过诱导染色质修饰酶或调控翻译、信号传导等经由发达作用,如GAS5、Lethe等已被阐述参与糖尿病猜想细胞调控。
商讨还发现,肥壮与T2DM可通过表不雅遗传重编程,影响脂质代谢、炎症响应等要津通路,进而激发微血管(肾病、视网膜病变、精神病变)和大血管(动脉粥样硬化)并发症,为DFU的发生埋下隐患。
三、细胞功能芜杂:表不雅遗传尽头的具体影响
01
免疫细胞:炎症响应失控,愈合程度停滞
免疫细胞是伤口愈合的“前锋部队”,其表不雅遗传尽头导致炎症响应过度且持久,成为DFU的中枢致病身分。
01
巨噬细胞:促炎表型锁定,无法转向树立
健康巨噬细胞会从促炎表型(Mφ1)滚动为树立表型(Mφ2),但T2DM患者巨噬细胞因多重表不雅遗传尽头被“锁定”在促炎现象:
(1)高血糖与肥壮通过SMYD3、SET7酶,在S100a9、S100a12等促炎基因脱手子区添加H3K4me3激活记号,亚搏app官方网站预设单核细胞为促炎表型;
(2)Setdb2酶抒发裁减,使IL-1β、TNF-α等促炎基因脱手子区H3K9me3扼制记号减少,基因不绝激活;
(3)Jmjd3酶去除H3K27me3扼制记号,强化促炎基因抒发;
(4)lncRNA GAS5上调STAT1,正向调控促炎基因。
02
T细胞:促炎表型偏移,免疫环境芜杂
T细胞是免疫调遣的中枢,其表不雅遗传尽头进一步加重伤口免疫芜杂:
(1)组卵白甲基鼎新酶MLL-1高抒发,调控Notch基因与RORγ基因抒发,使T细胞向促炎的Th17表型偏移;
(2)糖尿病现象下树突状细胞JARID1C基因抒发裁减,导致H3K4me3激活记号增多,IL-6、滚动孕育因子-β(TGF-β)分泌增多,进一步鞭策T细胞向Th17表型滚动;
(3)lncRNA ENST00000411554通过调控MAPK1信号通路,防止伤口免疫均衡。
02
结构细胞:树建功能瘫痪,伤口无法闭合
角质酿成细胞、成纤维细胞、内皮细胞看成“施工队”,其表不雅遗传尽头导致树立工程停滞。
01
{jz:field.toptypename/}角质酿成细胞:挪动受损
高血糖通过多重表不雅遗传机制扼制其挪动才气:
(1)Foxo1卵白调控Mmp9基因甲基化,TET2与GADD45a卵白激活Mmp9基因,过量MMP9防止ECM,影响挪动“支架”;
(2)伤口中IL-17α通过JMJD3酶扼制整合素α3抒发,整合素看成挪动“持手”,其穷乏进一步遏制上皮化。
02
成纤维细胞:滚动才气着落
成纤维细胞需滚动为肌成纤维细胞(抒发α-SMA)才气收缩伤口并构建树立骨架,但糖尿病现象下该经由受阻:
(1)TGF-β本应激活MLL-1酶调控α-SMA抒发,此表不雅遗传通路被阻断,肌成纤维细胞数目减少;
(2)lncRNA URIDS扼制PLOD1卵白活性,导致胶原卵白交联不及,ECM结构不清醒。
03
内皮细胞:血管荣达不及
内皮细胞酿成新毛细血管为伤供词能,但表不雅遗传尽头导致其功能瘫痪:
(1)高血糖上调Set7酶,通过H3K4me1激活促炎基因;
(2)DNMT3A与HDAC4酶扼制NOS3基因抒发,NOS3编码的eNOS是血管舒张与荣达的要津分子;
(3)Kdm7A、UTX酶激活NF-κB通路,加重炎症,扼制血管荣达。
四、商讨龙套:表不雅遗传靶向调理新标的
1.新式商讨时间:单细胞RNA测序、空间RNA测序、多组学聚首分析等时间,可无偏倚识别DFU中的新式细胞亚型,领会基因抒发与表不雅调控的关联,为精确靶点挖掘提供相沿。
2.表不雅遗传靶向后劲:商讨阐述,BRD9、JMJD3等表不雅遗传酶的扼制或调控,可改善巨噬细胞、角质酿成细胞等功能;针对lncRNA(如GAS5、URIDS)的侵犯,也可能矫正细胞尽头表型。
3.商讨缺口:结构细胞(尤其是成纤维细胞异质性、微血管内皮细胞)的表不雅遗传调控机制仍不解确,细胞间互作的表不雅遗传网罗有待进一步探索。
结语
DFU难愈的深层机制,在于高血糖等身分激发的表不雅遗传调控尽头,导致免疫细胞与结构细胞功能协同失调。巨噬细胞促炎表型“锁定”、角质酿成细胞挪动受阻、成纤维细胞滚动着落及内皮细胞血管荣达不及,共同遏制了伤口愈合的当然程度。当前商讨已揭示部分表不雅遗传靶点(如BRD9、JMJD3),将来诱导单细胞与空间多组学时间,有望完结从机制领会到靶向侵犯的龙套,为DFU的精确调理开垦新路线。
参考文件:
Bauer TM, et al. Arterioscler Thromb Vasc Biol. 2025 May;45(5):632-642.